Una terapia génica pionera para tratar enfermedades asociadas al estrés del retículo endoplasmático
La Universidad de Barcelona (UB) ha recibido de la AGAUR una ayuda Producto de 150.000 euros para desarrollar una nueva terapia génica destinada a tratar el estrés del retículo endoplasmático (ER), una disfunción celular clave en múltiples enfermedades, desde trastornos metabólicos como la diabetes hasta el cáncer y diversas enfermedades genéticas raras. El proyecto está liderado por el Dr. Antonio Zorzano, catedrático del Departamento de Bioquímica y Biomedicina Molecular de la Facultad de Biología de la UB y miembro del IRB Barcelona. También participa en él el investigador de su equipo, Dr. Kevin Aguilar, como científico emprendedor, y la Dra. Deborah Naon como responsable científica del proyecto.
El primer objetivo terapéutico de esta innovadora estrategia es el déficit de alfa-1 antitripsina (AATD), una enfermedad hereditaria rara sin tratamiento efectivo que afecta a uno de cada 2.000–5.000 nacimientos y contribuye entre el 2–3% de los casos de enfermedad pulmonar obstructiva crónica (EPOC).
La causa del AATD es una mutación en el gen de la alfa-1 antitripsina (α1AT), que provoca que esta proteína se acumule en el hígado, desencadenando estrés del retículo endoplasmático —un orgánulo presente en las células humanas— y generando daño hepático y pulmonar. Las terapias actuales aportan la proteína α1AT a los pulmones mediante infusión intravenosa, pero no resuelven el daño hepático ni el estrés celular que origina la enfermedad. “Nuestro objetivo es desarrollar una terapia integral que aborde tanto los síntomas pulmonares como los hepáticos del AATD, mejorando los resultados clínicos de los pacientes con esta enfermedad”, explica el Dr. Zorzano.
“Se trata de un cambio de paradigma, ya que esta terapia génica no pretende reemplazar un gen, sino actuar mediante un mecanismo terapéutico que aborda directamente el estrés del retículo endoplasmático y restaura la comunicación entre los orgánulos celulares”, subraya el catedrático de la UB.
Los datos preliminares, tanto en modelos murinos como en modelos celulares de la enfermedad, indican que la terapia podría reducir la acumulación de la proteína en las células hepáticas y mejorar de forma global las manifestaciones clínicas.
Impacto potencial en muchas otras enfermedades
Dada la gran cantidad de patologías asociadas al estrés del retículo endoplasmático, esta estrategia terapéutica podría extenderse a un amplio abanico de enfermedades que comparten este mecanismo, ya sea como terapia única o combinada, especialmente en aquellas que actualmente no disponen de un tratamiento eficaz.
Gracias a la financiación recibida a través de la ayuda Producto, los investigadores podrán validar esta nueva estrategia en un modelo murino avanzado de AATD para demostrar su eficacia y compararla con las soluciones existentes. También analizarán su potencial en otras enfermedades vinculadas al estrés del retículo endoplasmático, así como la mejora de los sistemas de administración del futuro fármaco.
Contribución a los Objetivos de Desarrollo Sostenible
El proyecto contribuye a los Objetivos de Desarrollo Sostenible (ODS) de la Agenda 2030, ya que busca mejorar la calidad de vida en enfermedades raras sin tratamiento efectivo (ODS 3, Salud y bienestar), impulsa la innovación en terapia génica y biomedicina (ODS 9, Industria, Innovación e Infraestructura), fomenta la creación de empleo en biotecnología y reduce la carga económica sobre los servicios de salud (ODS 8, Trabajo decente y crecimiento económico), prioriza el uso de modelos preclínicos éticos y prácticas de investigación sostenibles (ODS 12, Producción y consumo responsables) y promueve la colaboración entre investigadores, clínicos y responsables políticos para acelerar la llegada de nuevas terapias a la sociedad (ODS 17, Alianzas para lograr los objetivos).
El proyecto, con número de expediente 2025 PROD 00173, se enmarca en la convocatoria Industria del Conocimiento en la modalidad “Ayudas Producto destinadas a la obtención de prototipos y a la valorización y transferencia de los resultados de investigación generados por equipos de investigación de Cataluña”.
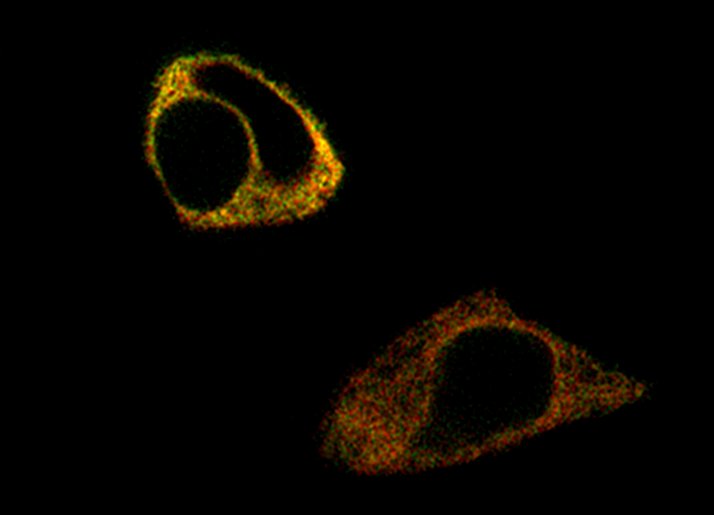
Pie de foto: La imagen muestra una célula hepática con un fenotipo normal en presencia del nuevo compuesto, a pesar de expresar la proteína mutada, que es la principal causa del AATD.

