Una teràpia gènica pionera per tractar malalties associades a l’estrès del reticle endoplasmàtic
La Universitat de Barcelona (UB) ha rebut de l’AGAUR un ajut Producte de 150.000 euros per desenvolupar una nova teràpia gènica per tractar l’estrès del reticle endoplasmàtic (ER), una disfunció cel·lular clau en múltiples malalties, des de trastorns metabòlics com la diabetis fins al càncer i diverses malalties genètiques rares. El projecte està liderat pel Dr. Antonio Zorzano, catedràtic del Departament de Bioquímica i Biomedicina Molecular de la Facultat de Biologia de la UB i membre de l’IRB Barcelona. També hi participa l’investigador del seu equip Dr. Kevin Aguilar, com a científic emprenedor, i la Dra. Deborah Naon com a responsable científica del projecte.
El primer objectiu terapèutic d’aquesta innovadora teràpia és el dèficit d’alfa-1 antitripsina (AATD), una malaltia hereditària rara sense tractament efectiu que afecta un de cada 2.000–5.000 naixements i contribueix a entre el 2–3% dels casos de malaltia pulmonar obstructiva crònica (MPOC).
La causa de l’AATD és una mutació del gen de l’alfa-1 antitripsina (α1AT), que provoca que aquesta proteïna s’acumuli al fetge, desencadenant estrès del reticle endoplasmàtic – un orgànul que es troba dins de les cèl·lules humanes – i generant dany hepàtic i pulmonar. Les teràpies actuals aporten la proteïna α1AT als pulmons mitjançant infusió intravenosa, però no resolen el dany hepàtic ni l’estrès cel·lular que origina la malaltia. “El nostre objectiu és desenvolupar una teràpia integral que abordi tant els símptomes pulmonars com els hepàtics de l’AATD, millorant els resultats clínics dels pacients amb aquesta malaltia”, explica el Dr. Zorzano.
“Es tracta d’un canvi de paradigma, ja que aquesta teràpia gènica no pretén reemplaçar un gen, sinó actuar mitjançant un mecanisme terapèutic que aborda directament l’estrès del reticle endoplasmàtic i restaura la comunicació entre els orgànuls cel·lulars”, subratlla el catedràtic de la UB.
Les dades preliminars, tant en models murins com en models cel·lulars de la malaltia, indiquen que la teràpia podria reduir l’acumulació de la proteïna en les cèl·lules hepàtiques i millorar globalment les manifestacions clíniques.
Impacte potencial en moltes altres malalties
Atesa la gran quantitat de patologies associades a l’estrès del reticle endoplasmàtic, aquesta estratègia terapèutica podria estendre’s a un ampli ventall de malalties que comparteixen aquest mecanisme, sigui com a teràpia única o combinada, especialment en aquelles que actualment no disposen d’un tractament eficient.
Gràcies al finançament rebut a través de l’ajut Producte, els investigadors podran validar aquesta nova estratègia en un model murí avançat d’AATD per demostrar-ne l’eficàcia i comparar-la amb les solucions existents. També analitzaran el seu potencial en altres malalties vinculades a l’estrès del reticle endoplasmàtic, així com la millora dels sistemes d’administració del futur fàrmac.
Contribució als Objectius de Desenvolupament Sostenible
El projecte contribueix als Objectius de Desenvolupament Sostenible (ODS) de l’Agenda 2030, ja que tracta de millorar la qualitat de vida en malalties rares sense tractament efectiu (ODS 3, Salut i benestar), impulsa la innovació en teràpia gènica i biomedicina (ODS 9, Indústria, Innovació i Infraestructura), fomenta la creació de llocs de treball en biotecnologia i redueix la càrrega econòmica sobre els serveis de salut (ODS 8, Treball digne i creixement econòmic), prioritza l’ús de models preclínics ètics i pràctiques de recerca sostenibles (ODS 12, Producció i consum responsables) i promou la col·laboració entre investigadores, clínics i responsables polítics per accelerar l’arribada de noves teràpies a la societat (ODS 17, Aliances per assolir els objectius).
El projecte, amb número d’expedient 2025 PROD 00173, s’emmarca en la convocatòria Indústria del Coneixement en la modalitat “Ajuts Producte destinats a l’obtenció de prototipus i a la valorització i transferència dels resultats d’investigació generada per equips de recerca de Catalunya”.
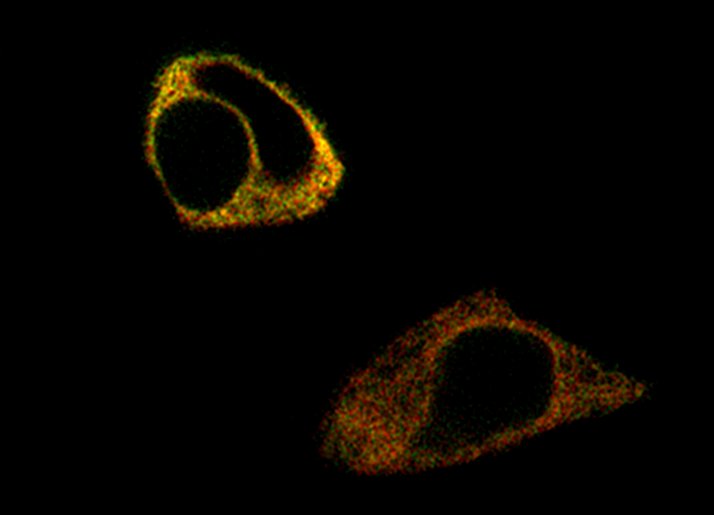
* Peu de fotografia: La imatge mostra una cèl·lula hepàtica que mostra un fenotip normal en presència del nou compost, malgrat expressar la proteïna mutada, que és la causa principal d’AATD.

